深圳三院成功构建人源肝脏类器官:完整复现HBV生命周期,慢性乙肝建模迎来"替身"时代
稿件来源:本网 发布时间:2026-04-09 11:00:54近日,深圳市第三人民医院(南方科技大学第二附属医院)卢洪洲教授与吴芬芳教授团队在国际学术期刊《BioScience Trends》上合作发表了一项重要研究成果。研究团队成功利用人诱导多能干细胞(hiPSC)构建了功能性肝脏类器官,该模型能够完整再现乙型肝炎病毒(HBV)的整个生命周期,并在体外模拟了慢性HBV感染相关的早期肝纤维化改变,为乙肝精准医学研究及抗病毒药物筛选提供了全新的“替身”平台。

论文创新点:
1. 建立hiPSC来源的多谱系肝类器官系统,通过定向共分化策略同时获得肝实质细胞和非实质细胞,重现肝脏复杂微环境。
2. 实现完整HBV生命周期模拟,包括病毒入胞、复制、cccDNA形成、抗原分泌及感染性子代病毒产生,突破传统模型局限。
3. 类器官在感染条件下长期存活达20天以上,NTCP受体稳定高表达,可持续分泌HBsAg和HBeAg,为慢性感染研究提供平台。
4. 首次在肝类器官中重现HBV感染诱导的肝纤维化病理特征,表现为COL1A1上调和肝细胞功能基因下调,模拟早期细胞外基质重塑。
5. 构建抗病毒药物筛选与肝毒性评估一体化平台,可区分替诺福韦和bulevirtide的不同作用机制,实现药效与安全性同步评价。
现有模型局限多,类器官带来新希望
HBV感染全球约2.96亿人,是导致肝纤维化、肝硬化及肝癌的主要病因。然而,传统研究模型长期存在瓶颈:动物模型存在种属特异性且成本高昂;肝癌细胞系无法反映正常肝细胞功能;原代人肝细胞来源有限且难以长期培养。这些模型均难以模拟HBV慢性感染过程及病毒与宿主间的动态相互作用。
为解决这一难题,研究团队基于前期建立的肝-胆多谱系类器官技术,进一步开发出高表达HBV关键受体NTCP的人源肝脏类器官。该模型不仅包含肝实质细胞,还保留了非实质细胞成分,更接近人体肝脏的真实微环境(图1)。
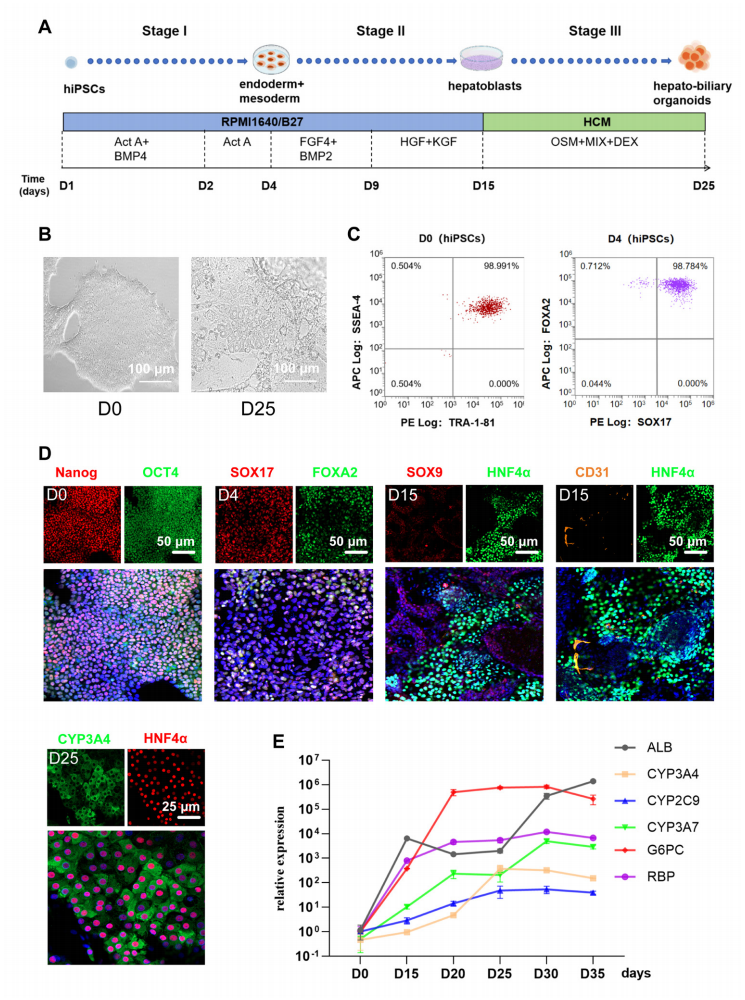
图1
完整模拟病毒生命周期,持续感染20天以上
研究显示,该类器官可支持HBV从进入、脱壳、复制、cccDNA形成、抗原分泌到感染性子代病毒产生的全过程(图2)。
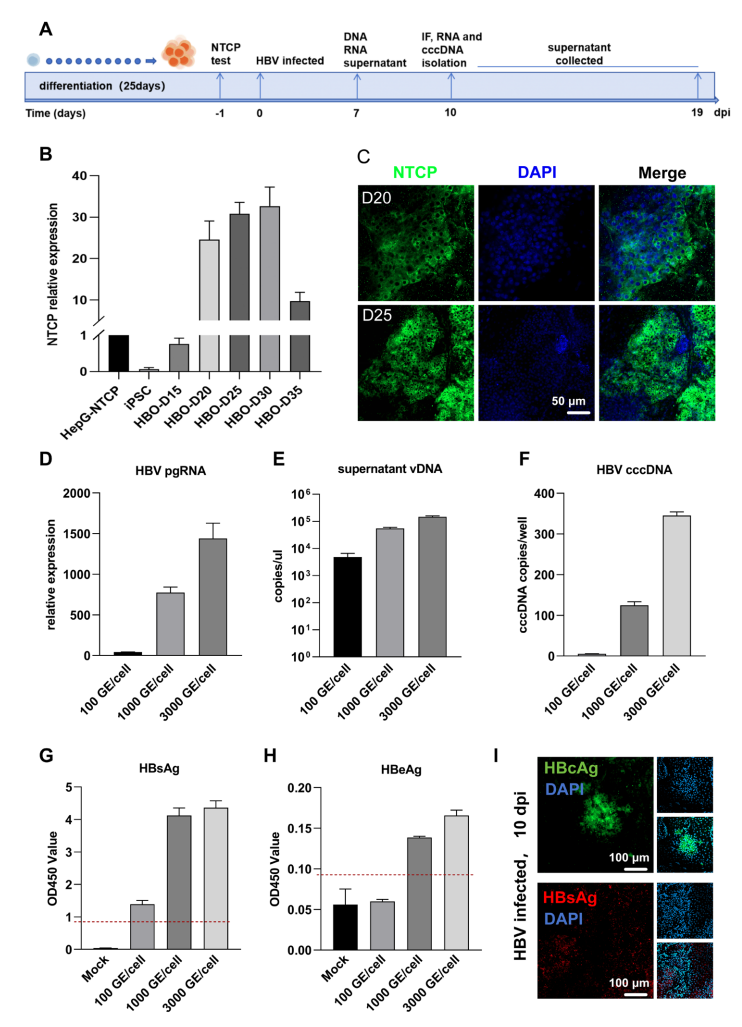
图2
感染后,类器官至少可维持活力与病毒复制达20天,并持续分泌HBsAg和HBeAg。免疫荧光检测证实,类器官中存在HBcAg和HBsAg的共表达。尤为重要的是,感染后的类器官呈现出肝功能障碍和早期纤维化样改变:功能相关基因(如ALB、CYP3A4等)显著下调,而纤维化标志物COL1A1表达明显升高(图3)。这是目前体外模型中少数能同时再现病毒感染与肝脏早期纤维化病理特征的系统之一。
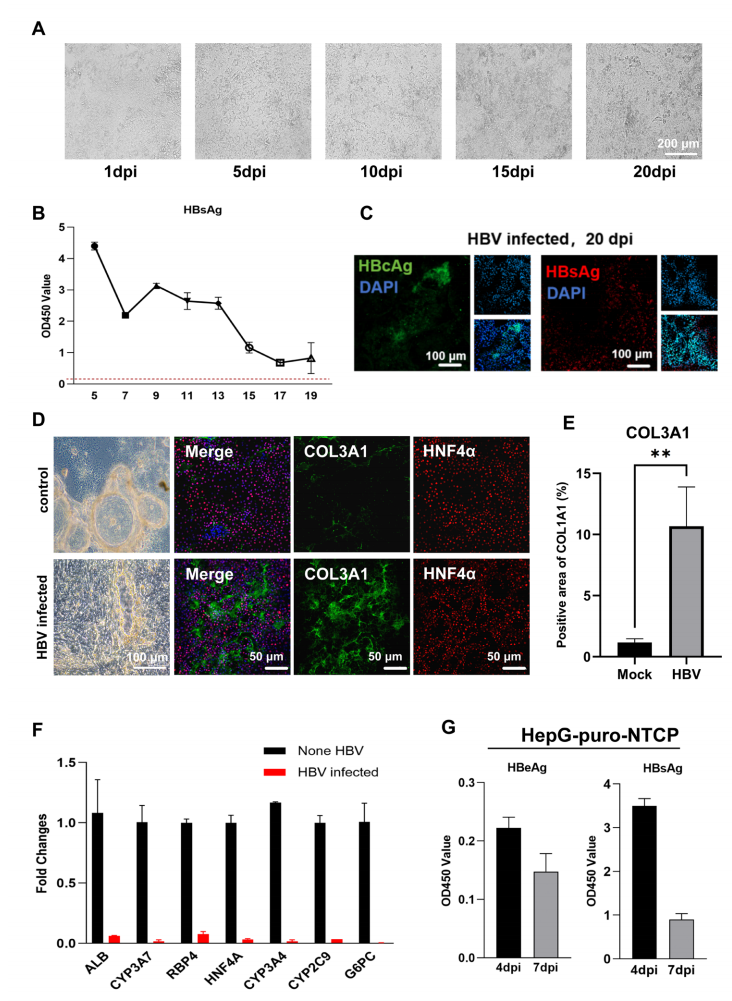
图3
药物评价:既能看疗效,又能辨机制
研究团队进一步验证了该模型在抗病毒药物筛选中的价值。使用临床常用药物替诺福韦处理感染后的类器官,可显著抑制病毒DNA和抗原分泌,但对cccDNA无影响,符合其作用机制;而使用HBV进入抑制剂布乐韦肽预处理,可有效阻断病毒感染,但感染后给药则无效,清晰体现了其阶段特异性抑制作用。此外,该模型还可同步评估药物的肝细胞毒性,为临床前药物安全性评价提供了更接近人体的参考体系(图4)。
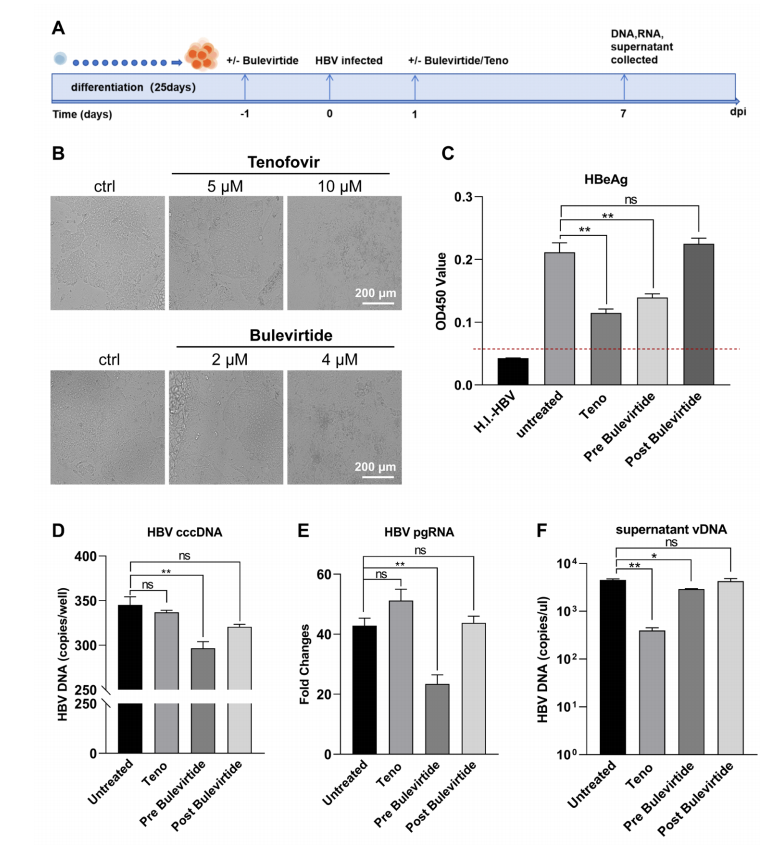
图4
从“替身”到“利器”,推动乙肝研究与新药研发
该hiPSC来源的肝脏类器官模型,兼具人源性、可规模化、可长期培养、支持完整病毒生命周期且能模拟纤维化等多重优势,弥补了传统细胞系和动物模型之间的空白。这不仅是慢性乙肝体外建模的重大突破,更为抗乙肝新药的研发与筛选提供了一个“全生命周期、全病理过程”的高效平台。
深圳市第三人民医院博士后刘谭彬为论文第一作者,中山大学附属八院博士生徐俊明为共同第一作者,深圳市第三人民医院院长卢洪洲教授、生物治疗中心负责人吴芬芳教授为该论文共同通讯作者,深圳市第三人民医院为论文完成第一单位。
该研究得到国家科技重大专项、国家重点研发计划、广东省新发传染病诊治重点实验室、深圳市传染病诊治技术重点实验室、深圳市重大新发突发传染病临床医学研究中心的资助。
附件:







 粤公网安备 44030702003859号
粤公网安备 44030702003859号
